刘志佳教授/陈永明教授团队在mRNA药物递送领域取得新进展
以信使RNA(mRNA)为代表的核酸药物,近年来在临床上取得了重要进展,应用范围涵盖预防性疫苗、肿瘤疫苗、基因编辑等多个领域。在当前的mRNA递送系统中,由可电离阳离子脂质(IL)、磷脂、胆固醇和聚乙二醇化脂质组成的脂质纳米颗粒(LNP)是最为成功的平台。两款广为人知的新冠mRNA疫苗(mRNA-1273和BNT162b)已获得美国食品和药物管理局(FDA)批准,正是采用这一LNP递送技术。在LNP的各组分中,IL是决定递送性能的关键。目前,以组合化学为核心的高通量筛选是IL开发的重要手段,但人们对IL结构与其mRNA递送性能之间的构效关系理解仍然有限,如何理性设计具有高递送效率和靶向特异性的LNP体系,仍是当前极具挑战的领域难题。
近日,我院刘志佳教授/陈永明教授团队基于前期提出的Ugi四组分反应(Ugi-4CR)用于器官靶向IL开发的积累(Angew. Chem. Int. Ed.2023, 62, e202310401),系统研究了IL异构化这一容易被忽视的材料结构设计对LNP递送性能的影响,揭示了其中关键的科学机制。Ugi-4CR是一种多组分反应,能够将醛、异腈、胺和羧酸四类反应所携带的官能团,在一步反应中构建到目标化合物中,是目前IL高通量筛选的重要方法。本研究在Ugi-4CR生成的α-酰氨基酰胺骨架基础上,选择一个N,N-二甲基丙基作为可电离阳离子头部,一个1-乙基戊基作为短链疏水尾部,以及两个(Z)-9-十八碳烯基作为长链疏水尾部,将这四种官能团与Ugi-4CR的四类反应物相匹配,成功获得了9种具有相同官能团但排列顺序不同的位置异构化IL(图1)。通过微流控技术将这些IL制备成LNP并开展性能表征,研究发现不同头部异构化IL会显著影响LNP的表观pKa值。进一步结合分子动力学模拟和小角中子散射技术,研究揭示了分子间相互作用如何影响异构化IL在LNP中的分布,进而决定LNP表观pKa的内在机制,从分子层面阐明了IL结构如何决定LNP的性质(图2)。最后,该研究还证明,IL异构化的LNP通过不同给药方式,能够调控mRNA在体内的器官及细胞靶向递送性能。这一工作为开发下一代高效、精准、安全的mRNA药物递送系统提供了关键方案。
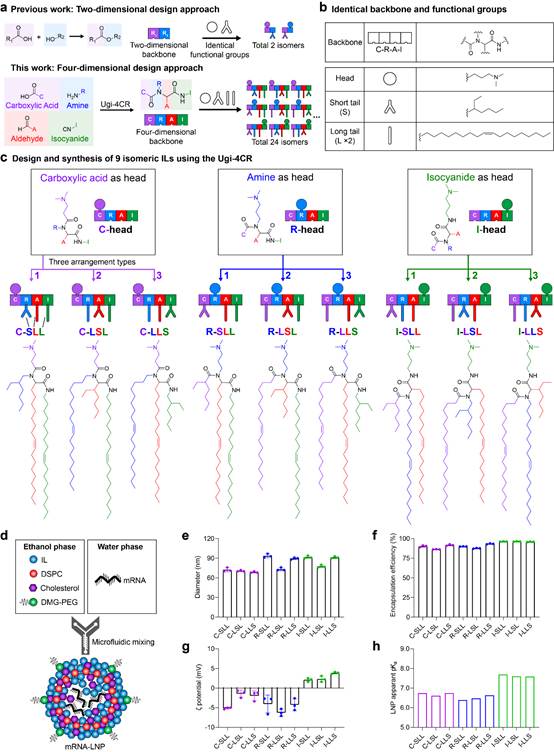
图1. (a-c)基于Ugi-4CR的异构IL设计;(d-h)通过微流控技术制备异构IL的LNP并进行性能表征
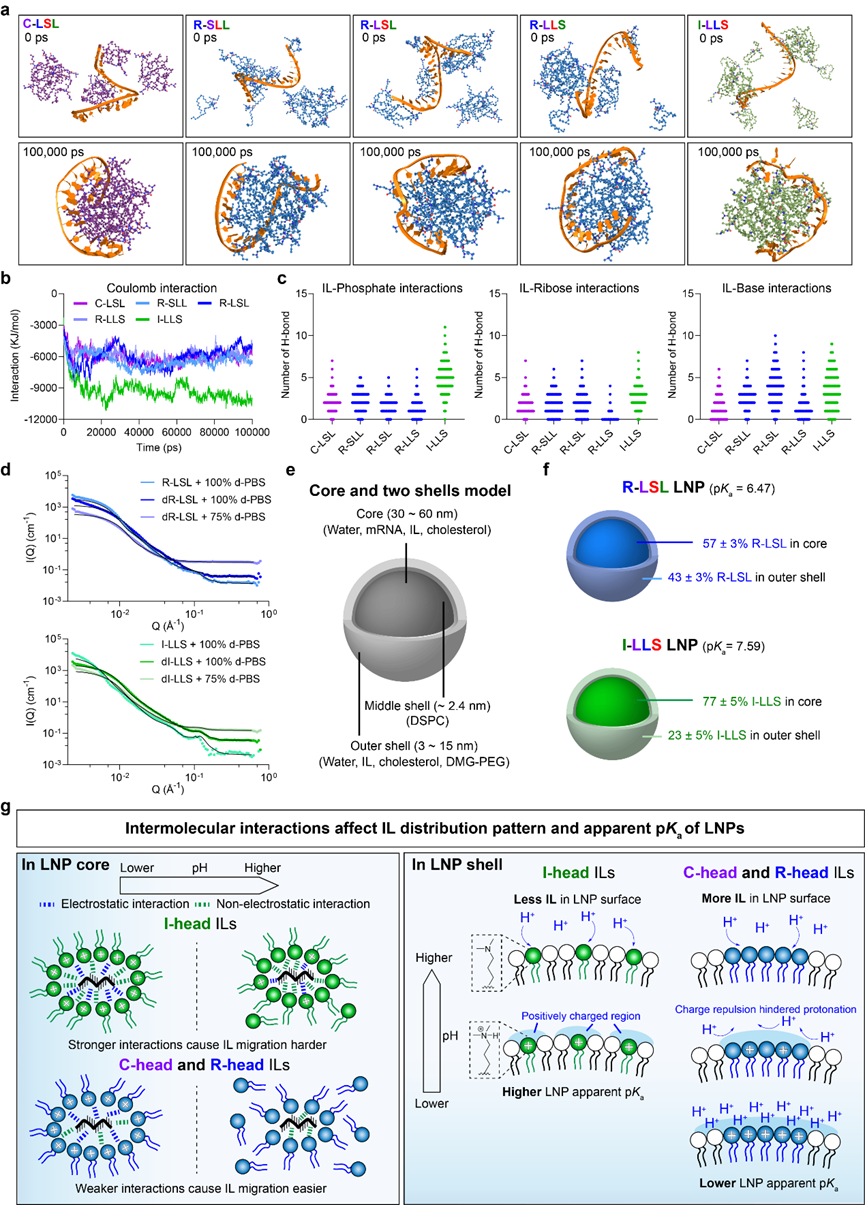
图2. (a-c)通过分子动力学模拟研究异构IL与mRNA的相互作用;
(d-f)通过小角中子散射研究异构IL在LNP中的分布情况;(g)异构IL影响LNP的表观pKa的分子机制
该成果于2026年3月11日以“Unraveling the Role of Ionizable Lipid Isomerism in Modulating Lipid Nanoparticles for mRNA Delivery”为题,正式发表于期刊Journal of the American Chemical Society (J. Am. Chem. Soc.2026, 148, 9596–9607. https://doi.org/10.1021/jacs.5c20438)。中山大学材料科学与工程学院为论文第一完成单位。我院2020级博士生贺泽芃为论文第一作者,中山大学刘志佳教授、陈永明教授,中国科学院高能物理研究所及东莞散裂中子源科学中心程贺研究员为通讯作者。该工作得到国家自然科学基金以及省、市基金项目的支持。
初审:袁湛楠
审核:田雪林、许俊卿
审核发布:李伯军



