陈永明教授/刘利新教授团队在自身免疫病抗炎治疗领域取得新进展
核酸酶(DNase)功能缺失可以使体内核酸异常堆积进而导致疾病发生,如在系统性红斑狼疮患者中DNase酶严重缺失使患者体内游离核酸(cfDNA)水平异常增高,先天免疫受体TLR9被激活产生炎症因子,造成组织损伤。在前期研究中,西班牙学者María A Moro通过补充DNase I降解cfDNA有效缓解了缺血性脑卒中模型小鼠的症状。在临床上,重组DNase I已被批准用于囊性纤维化(cystic fibrosis,CF)慢性长期治疗。但本团队研究发现,采用CF相同剂量的DNase I静脉给药,RA模型大鼠炎症反应未能有效缓解。提高DNase I给药频率和浓度,RA模型鼠炎症症状才得以部分缓解。与发表文献不同的结果激发我们去探索在自身免疫性疾病中,异常增高的cfDNA不能被DNase有效降解的机制。
我们考虑到在自身免疫性疾病中,cfDNA往往与体内的蛋白或者多肽如:HMGB1,抗cfDNA IgG、LL37形成免疫复合物(ICs),推测ICs阻碍DNase对DNA的降解。我们以LL37为模型多肽,采用分子动力学模拟对DNase I-DNA二元复合物与DNase I-DNA-LL37三元复合物进行结合能力与结构特征的分析。结果发现LL37的引入破坏了DNase I 与DNA的结合,在DNase I-DNA二元复合物中,其催化结构域中关键残基His-252可以高亲和力结合DNA。但在DNase I-DNA-LL37三元复合物中,LL37使催化结构域α碳运动幅度显著增大,降低底物与DNase I结合自由能。此外,通过计算,发现 LL37破坏DNase I结构稳定性。由此,解释了在自身免疫性疾病中,即使高剂量、高频度使用DNase,仍无法有效缓解模型鼠的炎症反应(图1)。
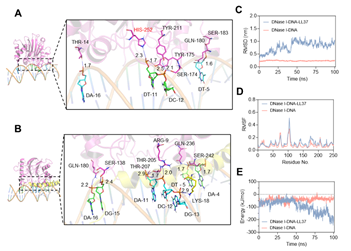
图1. 二元与三元复合物的分子动力学模拟
针对以上结果,我们提出用阴离子糖胺聚糖肝素(heparin)作为ICs解离剂的新型治疗策略。采用肝素通过电荷相互作用竞争性与LL37结合,将cfDNA从ICs中置换释放,恢复DNase I对cfDNA的有效降解,科研设想被实验结果验证有效。考虑到游离DNase在体内容易被降解,无法有效到达炎症部位的局限性。我们采用单宁酸,通过氢键驱动自组装负载DNase I,制备成纳米颗粒(DNase@TANP),赋予其炎症靶向富集、pH响应缓释等特性,有效克服了游离DNase I半衰期短、病灶富集不足的问题。通过序贯给药(先注射肝素,30分钟后注射DNase@TANP),RA模型大鼠在第27天实现后肢体积完全恢复(图2)。关节腔内TNF-α、IL-6及cfDNA水平显著降低,H&E染色显示炎症细胞浸润消失、软骨边界恢复、骨侵蚀得到有效控制,IL-6及IL-1β免疫组化染色接近正常水平。
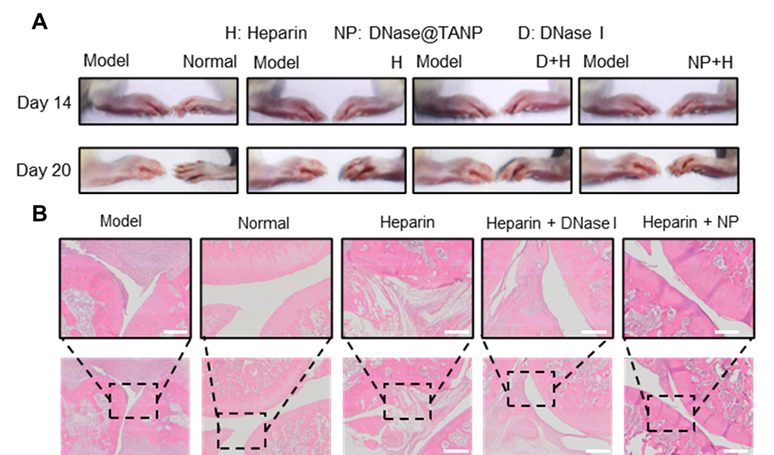
图2. 肝素与 DNase@TANP 联合策略治疗RA模型大鼠
由此,本项研究首次完整阐明了LL37-cfDNA-DNase I三元复合物的形成机制以及对DNase I活性的双重抑制原理,解答了为何类风湿关节炎中单纯施加DNase I治疗效果有限这一科学问题。在此基础上提出的先剥离、后降解序贯策略,构建了一种协同互补的cfDNA清除范式。肝素、DNase I是在临床上已被批准使用的药物,该治疗策略具备潜在的临床转化基础(图3)。
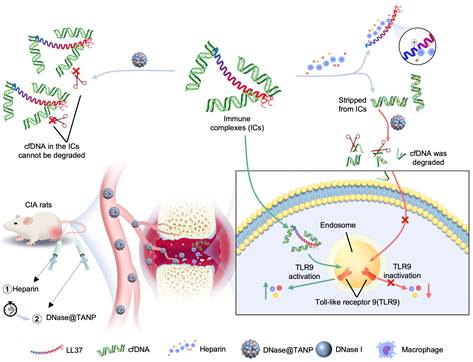
图3. DNase@TANP与肝素联合给药,通过靶向解离并酶促降解免疫复合物中的cfDNA抑制RA进展
该工作以“Stripping cell-free DNA from its immune complex is essential for inflammation control using DNase I”为题发表在国际期刊《Biomaterials》上(Biomaterials, 2026: 123992.,doi.org/10.1016/j.biomaterials.2026.123992)。我院2022级博士研究生陈实为第一作者,我院陈永明教授、刘利新教授及中国药科大学刘兴亮副研究员作为论文的共同通讯作者,中山大学材料科学与工程学院为论文第一完成单位。该研究工作受到国家自然科学基金支持。
文章链接:doi.org/10.1016/j.biomaterials.2026.123992
初审:袁湛楠
审核:田雪林、许俊卿
审核发布“李伯军”



